科大以嶄新合成生物學方法 破解大腸桿菌素致癌的機制 有助研究預防大腸癌方法
2019-09-17
 錢培元教授(右)及其研究團隊成員李忠瑞利用圖右的儀器培植細菌
錢培元教授(右)及其研究團隊成員李忠瑞利用圖右的儀器培植細菌
香港科技大學(科大)一個跨學科研究團隊發現,人體腸道中大腸桿菌所釋出的一種毒素,與大腸癌有關。研究不但為大腸桿菌對人類健康的影響帶來新見解,更有助推動預防全球第三常見癌症「大腸癌」 的研究*。
人體腸道中的大腸桿菌雖然可以幫助我們消化食物及調節免疫系統,但它們亦含有毒性,可以導致細胞周期停滯(arrest cell cycle)甚至死亡。科學家早已發現大腸桿菌所產生的大腸桿菌素(Colibactin)是一種基因毒性(genotoxin)化合物,可以破壞真核細胞中脱氧核醣核酸(DNA)的雙螺旋結構(double-strand breaks),增加患上大腸癌的風險。不過,由於這種化合物濃度低、狀態不穩定及生物合成反應路徑(biosynthetic pathway)過於複雜,難以複製作研究用途,所以它到底如何導致DNA受損,至今仍是一個謎。
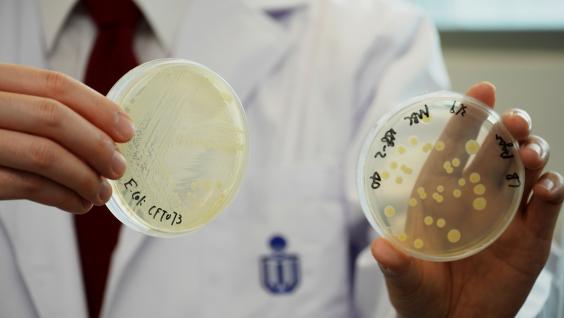 圖左是研究團隊培植的大腸桿菌
圖左是研究團隊培植的大腸桿菌
由科大捷成 David von Hansemann 理學教授、海洋科學系及生命科學部講座教授錢培元帶領的研究團隊,利用嶄新的生物合成方式,解開這個謎團。團隊不僅成功複製大腸桿菌素基因簇,更發現可以大量培植相關基因的方法,以進行測試及驗證。經過反覆分析及化驗多種大腸桿菌素前體化合物(Colibactin precursors),團隊最終確定「大腸桿菌素-645」是引致DNA雙螺旋結構受損的元兇,並發現其生物合成反應路徑和損害DNA雙螺旋結構的機制。
錢教授表示﹕「雖然部分大腸桿菌素會透過交叉連接的方式損害DNA,但一直以來未有資料顯示它們會直接破壞DNA。我們的研究確認了大腸桿菌素-645會直接破壞DNA的雙螺旋結構,進一步解釋大腸桿菌素對健康的影響,補上長久以來缺失的一塊拼圖。」
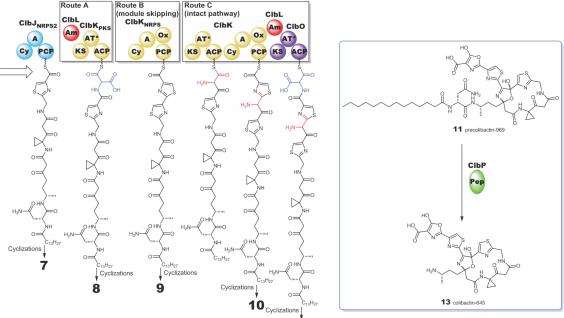 「大腸桿菌素-645」的生物合成反應路徑
「大腸桿菌素-645」的生物合成反應路徑
硏究團隊中的李忠瑞指,重組大腸桿菌素的分子骨架,可以為設計及合成有效的DNA分解試劑(DNA cleaving agent),例如合成限制性内切酶或癌症化療藥物提供基礎。
是次研究由科大、加州大學柏克萊分校及加州大學聖迭戈分校斯克里普斯海洋學研究所合作進行,研究結果已於國際權威科學期刊《自然 — 化學》中發表。此外,研究團隊早期就大腸桿菌素的研究成果也發表於國際權威科學期刊《自然 — 化學生物學》。
*根據世界癌症研究基金會2018年的統計數據: https://www.wcrf.org/dietandcancer/cancer-trends/colorectal-cancer-statistics
有關香港科技大學
香港科技大學(www.ust.hk)是國際知名的研究型大學,其科學、工程、商業管理及人文社會科學領域,均臻達世界一流水平。科大校園國際化,提供全人教育及跨學科研究,培育具國際視野、創業精神及創新思維的優秀人才。科大的研究於香港的大學教育資助委員會「2014研究評審工作」獲得最多「世界領先」評級,亦於最新的《泰晤士高等教育全球年輕大學排名榜2019》中排行第一,而科大的畢業生在2018年度的全球大學就業能力調查排名第16位,位列大中華院校之首。












 圖左是研究團隊培植的大腸桿菌
圖左是研究團隊培植的大腸桿菌 「大腸桿菌素-645」的生物合成反應路徑
「大腸桿菌素-645」的生物合成反應路徑

